Bromid
Nachweis von Bromid
Nachweis mit Schwefelsäure
Die Ursubstanz wird auf eine Tüpfelplatte gegeben und anschliessend einige Tropfen konz. Schwefelsäure zugegeben. Braune Dämpfe zeigen die Anwesenheit von Bromid.
Die Unterscheidung neben Iodid oder Nitrat/Nitrti (nitrosen Gasen) ist oft nicht ganz eindeutig.
Nachweis von Iodid, Bromid nebeneinander
In ein Reagenzglas wird die Probelösung gegeben un etwa mit 1 cm n-Heptan überschichtet. Danach wird mit Chlorwasser oder Chloramin-T unterschichtet. Aufgrund der Oxidationsfähigkeit des Chlors werden Iodid und Bromid oxidiert, steigen auf und lösen sich in der organischen Phase und sind anhand der Farbe zu erkennen. Sind beide in der Probe enthalten, so färbt diese sich oben violett und unten braun, die Farben sind jedoch nicht mehr eindeutig zu erkennen.
Nachweis von Chlorid, Iodid, Bromid nebeneinander
Die geloeste Ursubstanz wird mit Salpetersaure angesaeuert und anschliessend Silbernitrat zugegeben.
Der Niederschlag wird abzentrifugiert und anschliessend mit verduennter Ammoniakloesung versetzt.
Es wird erneut zentrifugiert und die Phasen voneinander getrennt. Die Loesung wird anschliessend wieder mit Salpetersauere angesauert. Ein weisser Niederschlag zeigt Chlorid an.
Dieser loest sich wieder beim Zugeben von 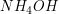 . Der zuvor abgetrennte Feststoff wird mit konz. Ammoniaklösung versetzt, die Phasen getrennt und die entstehende Loesung wieder angesauert. ein blassgelber Niederschlag zeigt Bromid an, welcher sich wiederum in konz. . Der zuvor abgetrennte Feststoff wird mit konz. Ammoniaklösung versetzt, die Phasen getrennt und die entstehende Loesung wieder angesauert. ein blassgelber Niederschlag zeigt Bromid an, welcher sich wiederum in konz. 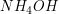 löst. löst.
Löst sich der urspruengliche Niederschlag nicht vollständig (gelber Rückstand, so ist Iodid nachgewiesen.
|